Arsenik elementinin sembolü “As” ve atom numarası 33’tür. Periyodik tablonun 33. sırasında yer alan arsenik, kükürt ve metallerin bir arada yer aldığı birçok mineralde, saf halde yer almaktadır. Arsenik elementi, saf element kristali halindedir ve metaloid özelliğe sahiptir. Gri form endüstrisine uygun olan arsenik, birden fazla allotropa sahiptir. Arsenik elementinin birincil kullanım alanı, kurşun alaşımlarının yer aldığı materyallerdir. Araba aküsü ve mühimmatlar, bu alaşımlara örnektir. Yarı iletken elektronik aygıtlar için “n” tipi dopant özelliğindedir optoelektronik bileşik ve galyum arsenit, katkılı silikonun ardından en fazla tercih edilen yarı iletken hükmündedir. Arsenik Nedir konusuna kısaca değindik. Şimdi biraz daha detaya ineceğiz.
İçindekiler
Arsenik Özellikleri Nelerdir?

Arsenik elementi fiziksel görünümü, gri, siyah ve sarı renklere sahiptir. Arsenik elementinin en yaygın 3 arsenik allatropu, gri, siyah ve sarı görünümündedir. En yaygın arsenik görünümü, gri renktedir. Birden fazla halkanın birleşiminden oluşan arsenik yapısı, birbirine kilitlenmiş dalgalı altı elemandan meydana gelmektedir. İki katmanlı yapıdadır ve katmanlar arasındaki bağlantı zayıflığı sebebiyle, gri arsenikler diğerlerine kıyasla daha kırılgan yapıya sahiptir. Çift katman yapısında yer alan 3 atomu, sıradaki üç atomdan daha yakın şekilde dizilmiştir. Sıradan giden en yakın komşular, çarpık oktahedral kompleks sistemini oluşturmaktadır. 5.73 g/cm3 yoğunluktaki sistemi, yakın paketleme sebebiyle maksimum yoğunluk oluşturmaktadır. Yapıda yer alan gri arsenik, semimetal özellikte olsa da amorfize edilmesi durumunda 1.2 – 1.4 eV bant aralığına dahil olarak, yarı iletken pozisyona geçmektedir. Sarı arsenik, kolayca şekil değiştirebilir ve yumuşak yapıdadır. Sarı arsenik yapısı, tetrafosforla benzerlik göstermektedir. Gri arsenik ise en stabil yapıdadır ve her iki arsenik de kolay bağlantı kurması için 4 yüzlü yapıdadır. Gri ve sarı arsenik, 3 atoma tek bağlantıyla sabitlenebilen 4 atoma sahiptir.
Pedagoji ne demek? Bilgilerini de inceleyebilirsiniz.
Arsenik İzotopları
Arsenik elementinin izotopları, doğada kararlı tek izotoptan oluşan, monoisotopik yapıya sahiptir. 2003 yılında yapılan inceleme sonucunda, 60 ila 92 aralığında değişiklik gösteren atom kütlesine erişilmiş ve değişken 33 radyoizotop ile karşılaşılmıştır. 80 – 30 arası yarı ömrü bulunan izotopları, elde edilen atom kütlesi arasında en kararlısı olarak değerlendirilmiştir. Kararlı arsenikten daha düşük kütleye sahip olan arsenikler pozitif (+) yönlü bozulma eğiliminde bulunurken, daha ağır kütledeki arsenikler negatif (-) yönlü bozulma eğilimi göstermektedir. Arsenik elementi için atom kütlesi 66 ila 84 aralığında değişiklik gösteren, minimum 10 adet nükleer izomer tespit edilmiş ve kayıtlara geçirilmiştir. Arsenik izomerleri arasında en fazla kararlılık göstereni, 111 saniyelik yarı ömrü ile 68mAs elementidir.
Arsenik Kimyası
Arsenik elementinin kimyası, türdeşleri arasında daha hafif yapıda olan fosfor ile benzerlik göstermektedir. Fosfor ile benzer elektronegativite ve iyonlaşma enerjisini barındıran arsenik, ametaller içerisinde kolaylıkla kovalent moleküler bağ kurmaktadır. Kuru havada kaldığında stabil yapısını korusa da nemli hava ve buhara maruz kaldığında, bronz rengi ile altın rengi arasında lekeler oluşturmaktadır. Oluşturduğu lekeler, zaman içerisinde siyahlaşmakta ve yüzey tabakası oluşturmaktadır.
Hava ortamında ısıtıldığında, arsenik trioksitlere yükseltgenmekte ve reaksiyon oluşturmaktadır. Reaksiyon sonucunda oluşan dumanlar, sarımsak benzeri koku yayar. Ortaya çıkan kokunun tespit edilmesi için arsenoporit ve asenür minerallerine çekiçle vurulması sonucunda anlaşılmaktadır. Fosfor bileşenleriyle aynı yapıya sahip olan arsenik, oksijenle temas ettiğinde yanmaktadır. Arsenik trioksit ile arsenik pentoksitini oluşturmak için oksijenle temasında yanmaktadır. Arsenik pentaflorürü oluşması için de florinde yanma göstermektedir. Belli başlı arsenik bileşenleri ve arsenik elementi, atmosfer basıncıyla temas etmesi durumunda, 887 K (614 Santigrat Derece) süblimine olmaktadır. Arsenik kimyası, süblimine olması durumunda, araya karışan sıvı hallere geçiş yapmadan, doğrudan gaz halini almaktadır.
Arsenik Element Bileşikleri
Arsenik bileşikleri, periyodik tablo üzerinde aynı gruba mensup olan fosfor elementiyle benzerlik göstermektedir. Oksidasyon durumlarında yaygın benzerlik gösteren arsenik, alaşım ve metaller arası bileşik ve arsenürde yer alan arsenik oranı -3, arsenitler için +3, arsenatlar ve birçok organoarsenik bileşikler için +5 değerine sahiptir. Skutterudit mineralinde yer alan As3-/4 iyonlarının meydana getirdiği tablodan anlaşıldığı gibi, kendi arasında da bağ kurabilen bileşik türüdür. +3 oksidasyon oluşması durumunda, arsenik elementi sadece elektron çiftinin etkisini barındırmakta ve tipik piramidal görüntü oluşturmaktadır.
Parapsikoloji nedir? Hakkında detaylar yazımızdadır.
Arsenik İnorganik Bileşikleri
İnorganik arsenik bileşikleri arasındaki en basit tür, arsenik trihidat olarak belirlenmiştir. Oldukça zehirli olan Arsin (ASH3) bileşeni, yanıcı türde piroforik özelliğe sahiptir. Genellikle kararlı yapıdaki bileşik, oda sıcaklığına geldiğinde yavaş şekilde ayrıştırılmaktadır. Sıcaklık seviyesi 250 derece ila 300 derece aralığında olduğunda, arsenik ve hidrojen ayrışması hız kazanır. Işık, nem ve alüminyum gibi belli başlı katalizörler sonrasında, ayrışım hızı artmaktadır. Su ve arsenik trioksit oluşumunda, arsenik yapısı hava ile temas etmekte ve kolaylıkla okside olmaktadır. Okside haliyle benzerlik gösteren reaksiyonlar, selenyum ve kükürt üzerinden meydana gelmektedir. Su içerisinde kolay ve hızlıca çözülen arsenik formları, renksiz ve kokusuz yapıdadır. Çözülmesi esnasında renksiz, kristal ve kokusuz As2O3 ve As2O5 higroskopik asit çözeltileri meydana getirmektedir. Zayıf asidik yapıdaki arsenik, yeraltı suyundaki arsenik kirliliğinin sebebi sayılmakta ve birçok insanı etkilemektedir. Sentetik arsenat yapısı, Scheelenin yeşili, kurşun hidrojen arsenatı ve kalsiyum arsenatı içerisinde barındırmaktadır. Belirtilen 3 ayrı arsenik bileşikleri, tarım ilaçlarında, zehirlerde ve böcek ilaçlarında etkili olarak kullanılmaktadır. Arsenik asit ile arsenik arasında meydana gelen protonasyon özellikleri, fosforik asit ve fosfat arasındaki farklarla benzer özelliklere sahiptir.
Arsenik İle İlgili Video Anlatım
Arsenik Alaşımları
Arsenik elementinin alaşımları, 5 element halinde sıralanmaktadır. III – V yarı iletken sayılan gallium arsenit, indiyum arsenit ve alüminyum arsenit olarak sıralanan alaşımlar, 5 element niteliğindedir. GaAs üzerinden belirtilen değerlik elektron miktarıyla, bir çift Si atom sayısı aynı ölçülere sahiptir. İki elektronun bant yapısı, birbiriyle tamamen farklılık göstermektedir. Bant yapılarının farklılığı, kütle yapısındaki çeşitliliklere yol açmaktadır. Farklı kategorideki arsenik alaşımları için II – V arasında yarı iletken arsenit yapısı ele alınmaktadır.
Arsenik Organoarsenik Bileşikler
Organoarsenik bileşik yapısı, birden çok çeşide sahiptir. I. Dünya Savaşı süresince, kimyasal silah ajanı olarak belirtilen organoarsenik bileşikler, savaş sonrasında da kimyasal silahlarda kullanılmak üzere geliştirilmeye devam etmiştir. Deride kabarcık oluşumuna yol açan lewisite ve kusmaya sebep olan adamzit, kimyasal silah ajanlarına birer örnektir. Tarih boyunca ilgi konusu olan arsenik alaşımları ve bileşiklerinden biri olan Kakodilic asit, fosfor elementinde analog yapısı bulunmayan trioksitin metilasyonu sonucunda elde edilmektedir. Çevreye rahatsızlık veren kokusu sebebiyle, kokdil adıyla anılmaya başlanmıştır.
Arsenik Biyolojik Etkileri Esansiyel İz Element Özelliği
Arsenik biyolojik etkileri ele alındığında, tavuk, keçi ve hamster gibi hayvanlar üzerinde, esansiyel ize sebep olduğu kanısına varılmıştır. Esansiyel iz oluşturan elemen yapısına dair kanıtlar elde edilse de esansiyel fonksiyonu hakkında, gözle görülür bir mekanizmaya ulaşılamamıştır. Arsenik nedir konusunu detaylı incelemeye devam ediyoruz. Şimdi Arsenik zararları’na bakalım.
Arsenik Zehirlenmesi Nedir?
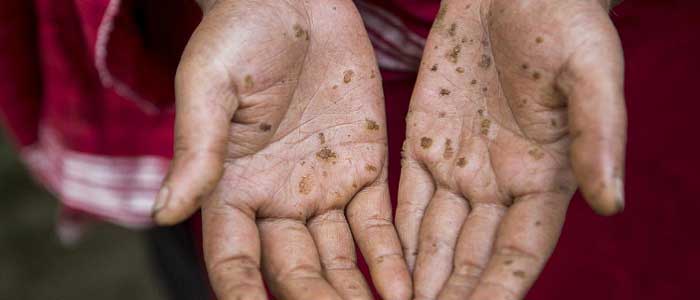
Arsenik zehirlenmesi, arsenik bileşiklerinin insan vücudundaki dokuları ve temel fonksiyonları etkilemesi sonucunda ortaya çıkmaktadır. Tarım ilaçları, böcek ilaçları ve benzer tüm zehirlerde yer alan arsenik, solunum yoluyla ve yutma yoluyla kişileri zehirlemektedir. Kanser ilaçları, boyalar, seramikler ve fare zehri gibi birçok ürünün temelinde, arsenik bileşeni yer almaktadır. Arsenik zehirlenmesi, bu türden maddelerin ağız ya da solunum yoluyla alınması durumunda kendini göstermekte ve ölümcül reaksiyonlar göstermektedir.
Ayrıca siber saldırı bilgilerini inceleyebilirsiniz.
Arsenik Nedir başlıklı içeriğimiz hakkında yorumlarınızı bekliyoruz.

